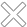Relevante Therapiefortschritte …
… beim Magenkarzinom
Die medikamentöse Therapie des Magenkarzinoms hat sich in den letzten Jahren deutlich verbessert. Zahlreiche Studien sowohl für die kurative als auch die palliative Situation zeigen beeindruckende Ergebnisse und haben den bisherigen Standard deutlich erweitert.
Neue Therapielinien konnten etabliert werden, und die Immuntherapie hat nun einen fixen Stellenwert in der Erstlinientherapie des metastasierten Magenkarzinoms.
Für das operable Magenkarzinom konnte die Prognose durch die Implementierung der perioperativen Chemotherapie deutlich verbessert werden. Die Überlebensrate für das mit kurativer Zielsetzung behandelte Magenkarzinom kann dadurch (gegenüber alleiniger Operation) mehr als verdoppelt werden. Die Entwicklung bleibt aber nicht stehen. Die Kombination mit zielgerichteten Substanzen für PatientInnen mit speziellen Biomarkern steht kurz bevor, der Einsatz von immunonkologischen Medikamenten für operierte PatientInnen, die zuvor eine Strahlen-Chemotherapie erhalten haben, wurde vor kurzem zugelassen.
Dennoch werden die meisten PatientInnen mit Magenkarzinom in einem inoperablen oder metastasierten Stadium diagnostiziert. Auch für diese PatientInnen konnte in den letzten Jahren (besonders im Jahr 2020) eine wesentliche Verbesserung erreicht werden: Zum einen durch die Etablierung von weiteren Therapielinien nach Versagen der Erstlinientherapie. In dieser Situation ist heute, im Gegensatz zu einem gewissen Therapie-Nihilismus vor Jahren, eine Zweit- und Drittlinientherapie etabliert. Durch die Einführung dieser Standards kann die Überlebenszeit, ganz wesentlich aber auch die Lebensqualität dieser PatientInnen signifikant und klinisch relevant verbessert werden.
Erfolg neuer Therapien beim Magenkarzinom
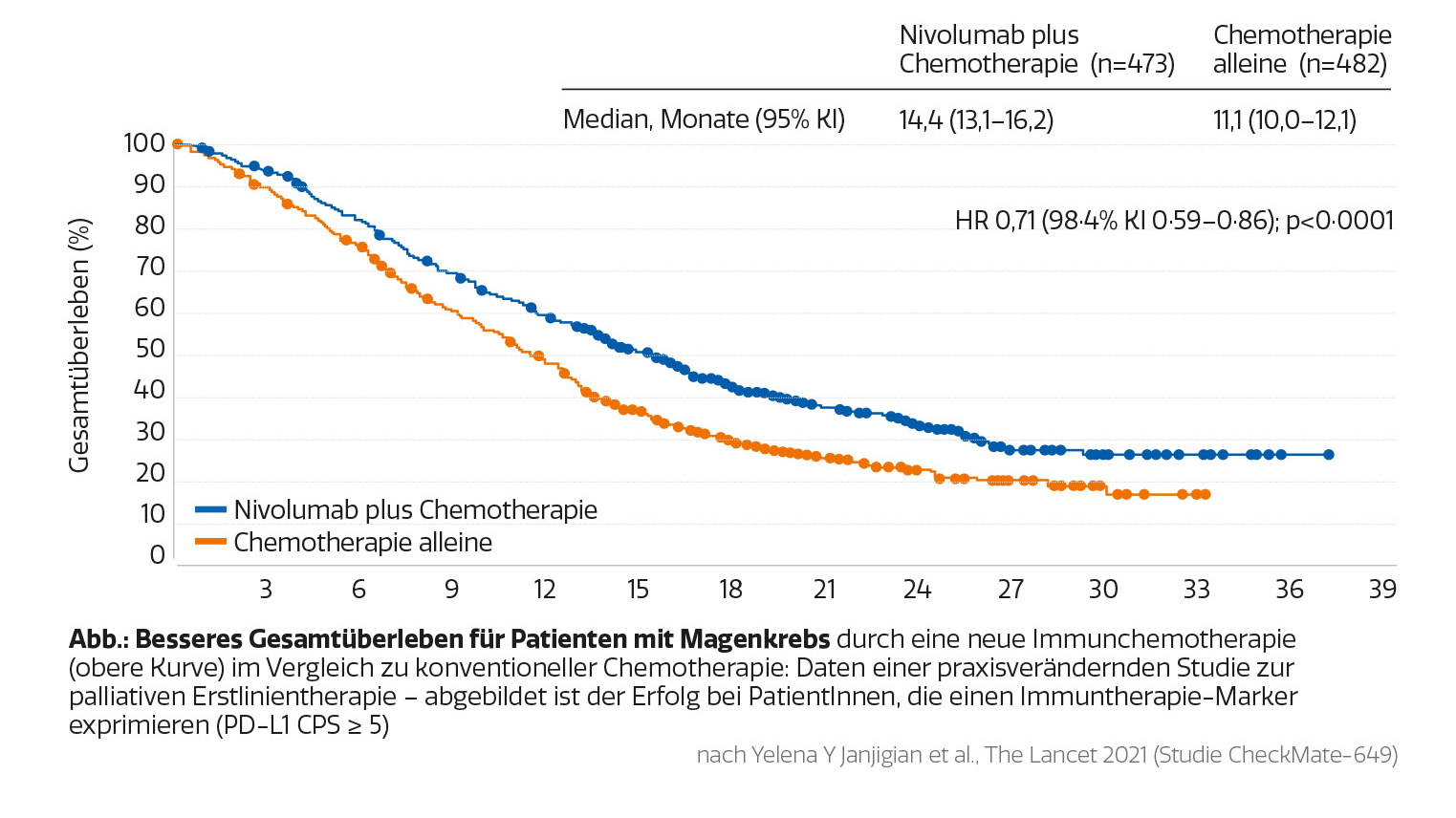
Zum zweiten ist eine bedeutende Innovation des letzten Jahres zweifelsfrei die Etablierung der Immuntherapie beim Magenkarzinom. Nachdem diese Therapie für selektionierte PatientInnen in späten Linien bereits zum Einsatz kam, konnte vor kurzem gezeigt werden, dass durch die Zugabe eines Immuncheckpoint-Inhibitors zur Chemotherapie in der ersten Therapielinie eine beeindruckende Verbesserung des Gesamtüberlebens erreicht wird. Aufbauend auf diesen Entwicklungen ist in den nächsten Jahren mit noch zielgenaueren Therapien, möglicherweise in Einzelfällen auch ohne klassische Chemotherapie, zu rechnen.
Ewald Wöll
… beim Lungenkarzinom
Das Lungenkarzinom stellt nach wie vor bei Männern die häufigste und bei Frauen die zweithäufigste krebsbedingte Todesursache dar. Dennoch ist die Indikation mittlerweile auch ein Paradebeispiel für die Entwicklung der modernen, zielgerichteten Onkologie. Beim frühen, nicht metastasierten Lungenkarzinom steht nach wie vor die Operation (ggf. gefolgt von einer Chemotherapie) im Mittelpunkt der Therapie, während beim fortgeschrittenen und somit nicht mehr heilbaren Lungenkarzinom eine möglichst personalisierte Behandlung erfolgt. Wichtig dafür ist die exakte Diagnostik aus einer Gewebeprobe des Tumors.
Diese beinhaltet neben der Bestimmung der histologischen Untergruppe (u.a. Plattenepithelkarzinom, Adenokarzinom, kleinzelliges Karzinom) auch eine Testung auf therapierelevante Biomarker wie PD-L1 für Immuntherapien und eine molekulargenetische Untersuchung auf aktivierende Mutationen im Tumorgewebe, die Angriffspunkte für zielgerichtete Medikamente darstellen (u.a. EGFR-, ALK-, ROS- oder BRAF-Inhibitoren).
Immuntherapie mit Checkpoint-Inhibitoren
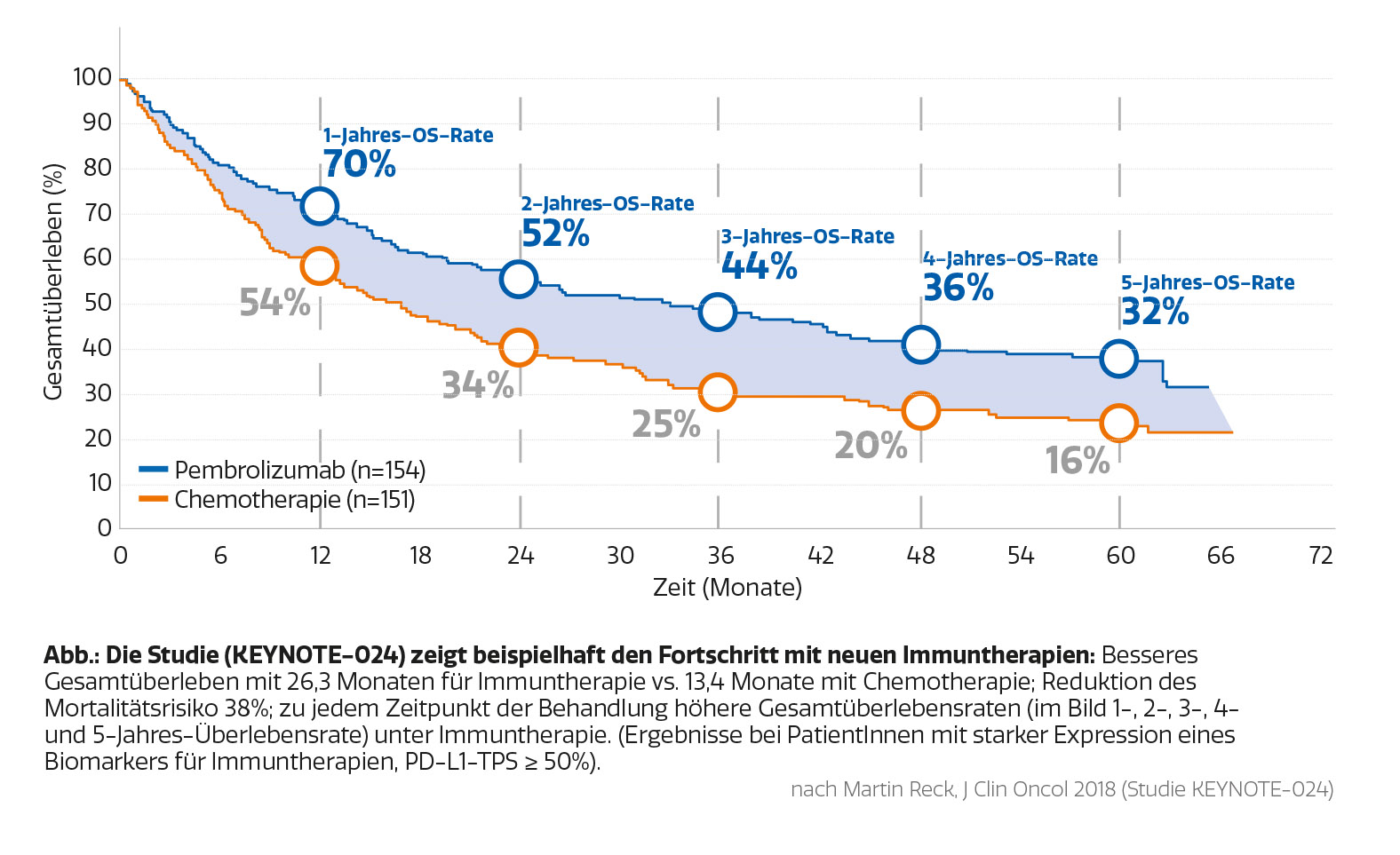
Die Immuntherapie mit Checkpoint-Inhibitoren hat sich zu einem wesentlichen Bestandteil in der Behandlung des fortgeschrittenen Lungenkarzinoms entwickelt. Sie führt zu einer (Re)Aktivierung des körpereigenen Immunsystems im Kampf gegen die Krebszellen. Die Immuntherapie wird je nach Ergebnis der Biomarkerbestimmung (z.B. Dichte der PD-L1-Expression auf Tumorzellen) alleine oder in Kombination mit Chemotherapie eingesetzt und führt zu einer Verlängerung der Überlebenszeit von PatientInnen mit Lungenkarzinom. Darüber hinaus sind die Nebenwirkungen einer Immuntherapie, verglichen mit Chemotherapie, deutlich geringer.
Immuntherapie mit einem Checkpoint-Inhibitor vs. Chemotherapie bei PatientInnen mit nicht-kleinzelligem Bronchialkarzinom
Zielgerichtete Therapie mit Tyrosinkinasehemmern
Bei ca. 15 % der PatientInnen mit Lungenkarzinom wird eine aktivierende Mutation in den Krebszellen gefunden. Diese PatientInnen kommen für eine zielgerichtete Therapie in Frage, die in der Regel mit Tabletten durchgeführt wird. Auch hier ist die Überlebenszeit deutlich länger und die Verträglichkeit besser als mit Chemotherapie. Die Forschung auf dem Gebiet des Lungenkarzinoms entwickelt sich rasant. Kannten wir vor drei Jahren nur vier therapierelevante Mutationen, so sind es jetzt zehn Mutationen, für die zielgerichtete Medikamente zur Verfügung stehen.
Gudrun Absenger
… mit CAR-T-Zelltherapie
Chimeric Antigen Receptor T-Cells (CAR-T-Cells) stellen eine neue immunologische Krebstherapie dar. Dabei werden Immunzellen des Patienten/der Patientin (T-Zellen) genetisch so modifiziert, dass sie an ihrer Oberfläche einen Antikörper exprimieren, der Krebszellen zielgerichtet erkennt und damit deren Zerstörung durch diese körpereigenen T-Zellen einleitet. Es handelt sich also gewissermaßen um einen „lebenden“ Antikörper, der auch über Jahre im Körper aktiv sein kann. Die Zellen werden zunächst mittels Apherese aus aus dem Patienten/der Patientin gewonnen, im Labor „scharf“ gemacht und anschließend, ähnlich wie bei der Stammzelltransplantation, zurückinfundiert. Das häufigste Target dieser Therapie ist das B-Zell-Antigen CD19. Damit können fast alle B-Zell-Lymphome behandelt werden. Zugelassen ist der Einsatz derzeit für rezidivierte aggressive Lymphome, Mantelzell-Lymphome und die akute lymphatische Leukämie des Kindes- und jungen Erwachsenenalters. Mit dieser Therapie verdoppelt sich das Langzeitüberleben der mehrfach vorbehandelten PatientInnen.
Erfolge mit CAR-T-Zell-Therapie
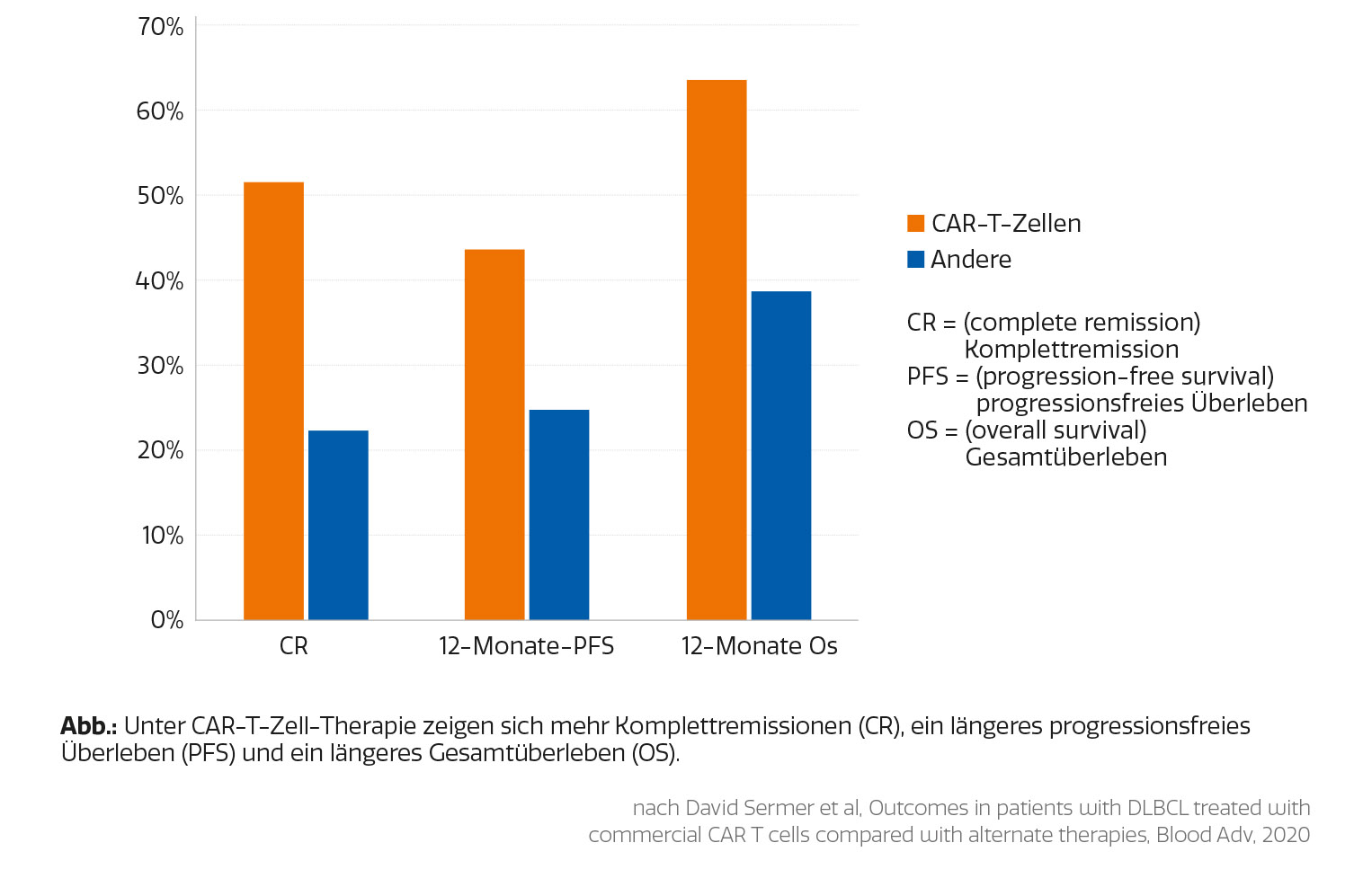
CAR-T-Zellen werden in klinischen Studien bereits gegen andere B-Zell-Lymphome, die chronisch lymphatische Leukämie, multiple Myelome sowie andere hämato-onkologische Erkrankungen geprüft. In Österreich hat sich das CAR-T-Zell-Netzwerk etabliert, das die sechs Zentren in Graz, Innsbruck, Linz, Salzburg und Wien umfasst. Im Austausch mit KollegInnen, Spitälern, Behörden und Trägern wurde ein umfassender Zugang zu dieser teuren Therapie für alle PatientInnen in Österreich auch regional sichergestellt. Die Netzwerkspitäler und Zuweiser kooperieren in Bezug auf Routinetherapien, klinische Studien und grundlagenwissenschaftlich. Regelmäßige Netzwerksymposien informieren Gesundheitsberufe, PatientInnen und die Öffentlichkeit (https://innere-med-1.meduniwien.ac.at/haematology/car-t-cell-network). In naher Zukunft sind die teilweise ambulante Therapie, Indikationserweiterung sowie eine mögliche Produktion vor Ort im Fokus. Auch bei den OeGHO-Tagungen wird regelmäßig über klinischen und wissenschaftlichen Fortschritt berichtet.
Ulrich Jäger
 Nutzung von Cookies: Wir benötigen Ihre Einwilligung
Nutzung von Cookies: Wir benötigen Ihre Einwilligung